今回は、中央社会保険医療協議会 総会(第649回)で取り上げられた、サンバイオの再生医療等製品「アクーゴ」について、資料の内容をもとに整理します。アクーゴは、外傷性脳損傷に伴う慢性期の運動麻痺の改善を対象とする新しい再生医療等製品であり、単なる新製品紹介にとどまらず、再生医療を公的医療保険の中でどう評価し、どう位置づけるかという制度上の重要な論点も含んでいます 1。
この記事では、スライドの流れに沿って、製品の基本情報、期待される作用、有効性データ、承認条件、そして保険上の取扱いまでを詳しく解説します。
この記事で押さえたいポイント
| 論点 | 要点 | 根拠 |
|---|---|---|
| 対象疾患 | 外傷性脳損傷に伴う慢性期の運動麻痺の改善を対象とする | 1 |
| 製品特性 | 遺伝子導入した間葉系幹細胞を用いる脳内移植製品である | 1 |
| 投与方法 | 定位脳手術と専用機器を用いた脳内投与が必要である | 1 |
| 有効性 | 24週時点のFMMS変化量で統計学的有意差が示された | 1 |
| 承認 | 条件及び期限付承認の下で追加評価が求められている | 1 |
| 保険上の整理 | 医薬品の例により対応し、薬価基準収載を審議する方向が示された | 1 |
アクーゴとは何か
「外傷性脳損傷に伴う慢性期の運動麻痺の改善」 1
中医協資料で示されたアクーゴの効能・効果又は性能は、上記のとおりです。ここで重要なのは、急性期治療ではなく、慢性期の運動麻痺を対象としている点です。慢性期は、一般に自然回復や通常のリハビリテーションによる大きな改善が得られにくく、治療選択肢の限界が意識されやすい領域です。そのため、この製品が評価されている背景には、未充足の医療ニーズの存在があります 1。

表紙スライドでは、今回のテーマが製品説明だけでなく、制度上の評価まで含むことを示しています。ブログ記事として読む際も、アクーゴを「再生医療の新薬」とだけ捉えるのではなく、高度な手技を伴う再生医療等製品が保険制度の中でどう扱われるのかという視点を最初に持っておくと、後の内容が理解しやすくなります。
スライド2:なぜこの製品が注目されるのか
アクーゴが対象とするのは、外傷性脳損傷に伴う慢性期の運動麻痺の改善です 1。この領域では、発症直後の救命や急性期管理とは異なり、一定期間を経た後に残る運動麻痺への対応が課題になります。患者にとっては、日常生活動作や社会復帰に直結する問題であり、家族や介護者にも大きな影響を与えます。
このスライドの意義は、アクーゴの話を始める前に、なぜこの製品が必要とされるのかを明確にしている点にあります。制度評価では、単に新規性があるだけでなく、既存医療で十分満たされていないニーズに応えるのかが重要です。慢性期の運動麻痺は、まさにその代表例の一つであり、アクーゴはその領域に対して新たな治療可能性を提示した製品として位置づけられます。
スライド3:アクーゴの製品概要
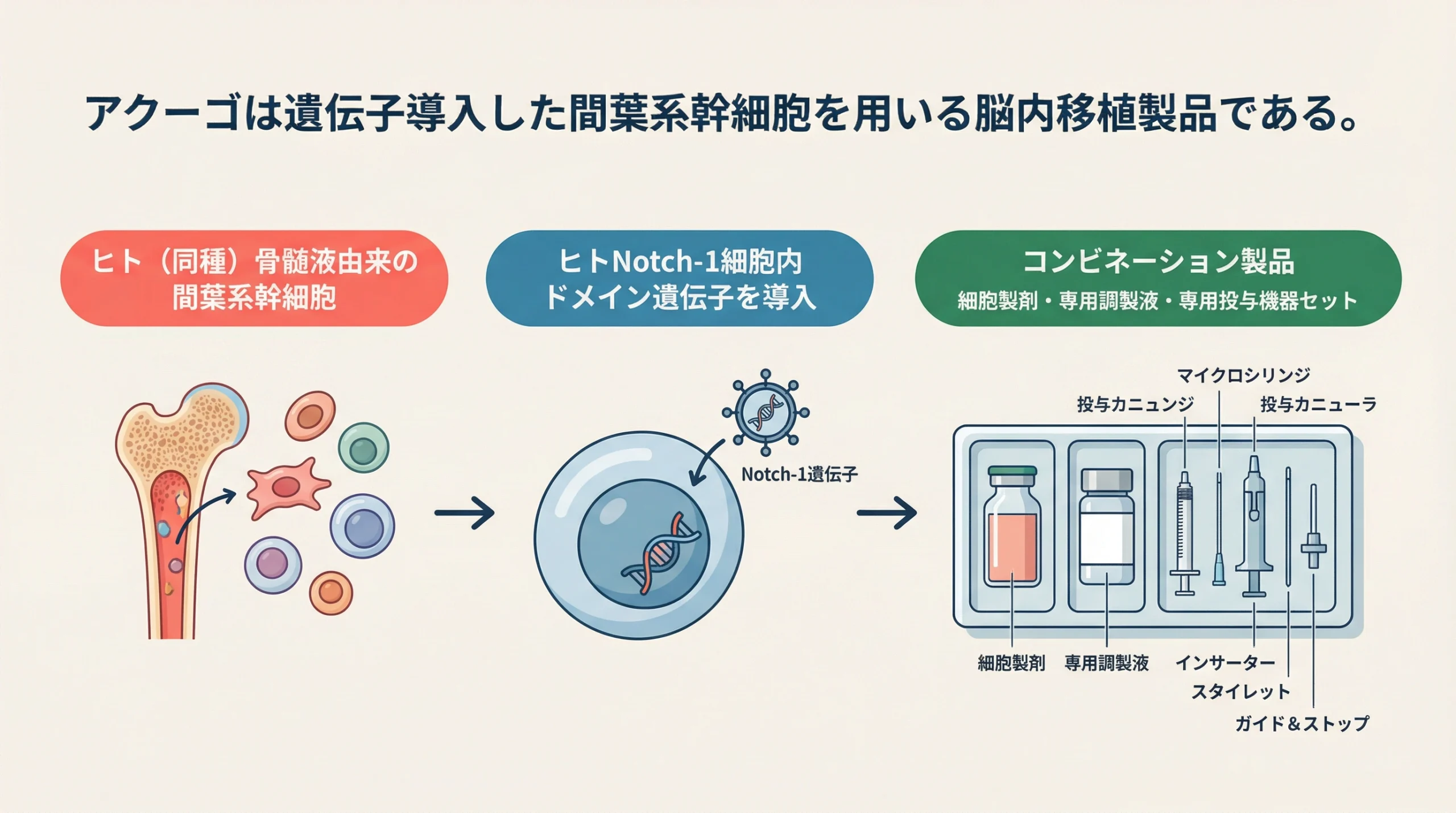
資料によると、アクーゴ脳内移植用注の一般的名称はバンデフィテムセルであり、健康成人から採取した骨髄液由来の間葉系幹細胞に、ヒトNotch-1細胞内ドメイン遺伝子を導入した細胞製品です 1。さらに、主構成体である脳内移植用細胞懸濁液に加えて、専用調製液と専用投与機器セットが副構成体として組み合わされています 1。
| 項目 | 内容 |
|---|---|
| 販売名 | アクーゴ脳内移植用注 |
| 一般的名称 | バンデフィテムセル |
| 類別 | ヒト細胞加工製品 |
| 承認区分 | 新再生医療等製品(希少疾病用再生医療等製品) |
| 収載希望者 | サンバイオ株式会社 |
ここで押さえたいのは、アクーゴが単独の「薬剤」ではなく、細胞、調製液、投与機器、外科的手技が一体化した治療システムに近いということです。したがって、品質評価や保険上の議論でも、通常の医薬品以上に製品そのものと使用方法の結びつきが強く意識されます 1。
スライド4:期待される作用機序
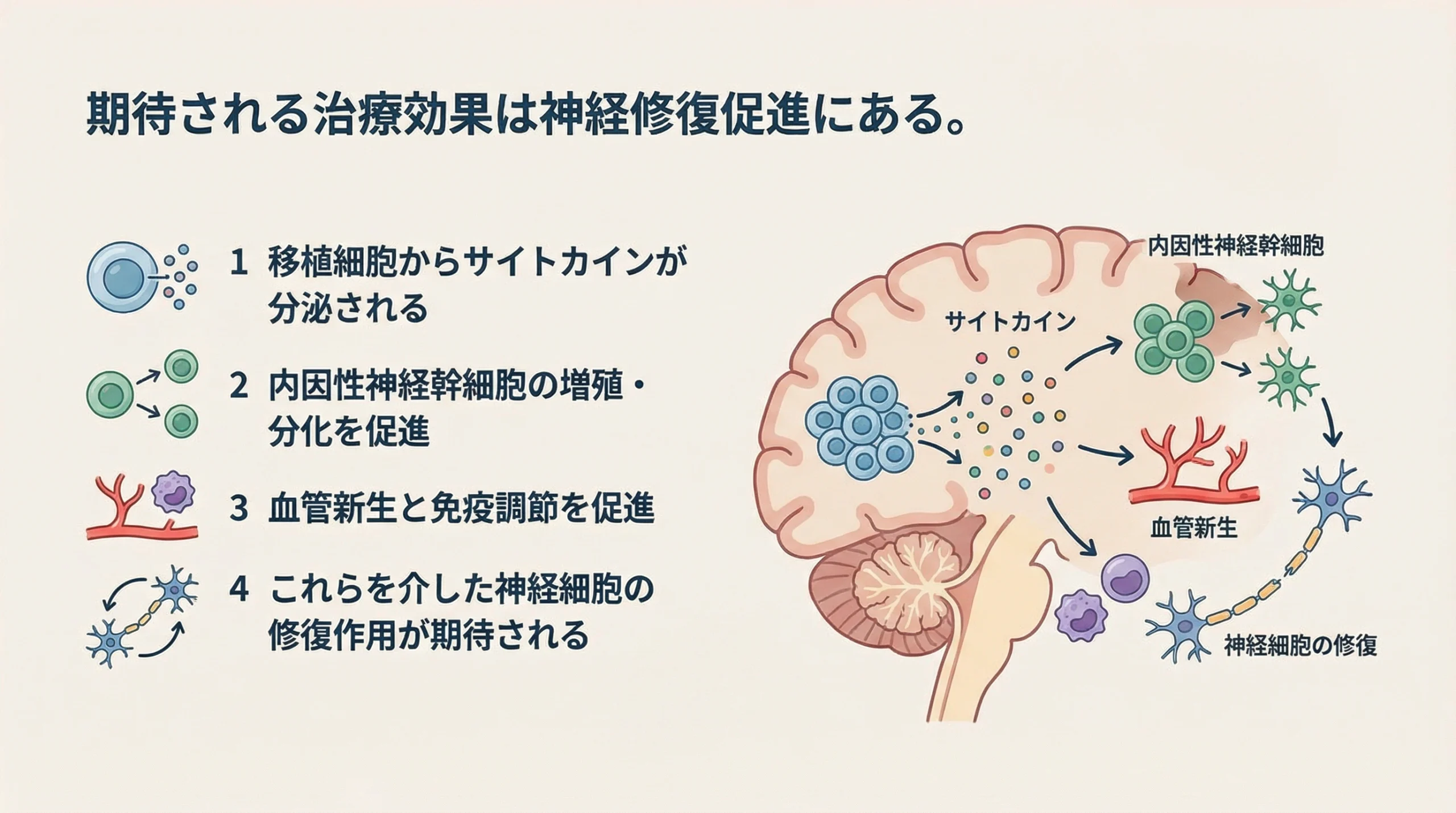
資料では、アクーゴの作用について、移植細胞から分泌されるサイトカインにより、内因性神経幹細胞の増殖・分化、血管新生、免疫調節促進などを介した神経細胞修復が期待されると整理されています 1。この説明のポイントは、単純に「失われた神経を置き換える」というより、脳が持つ修復反応を後押しする方向で理解されていることです。
この点は、再生医療を一般向けに説明するときに誤解されやすい部分でもあります。再生医療という言葉から、移植細胞がそのまま新しい神経組織になるようなイメージを持たれがちですが、中医協資料の整理は、より慎重で、生物学的作用を介した修復促進として位置づけています 1。制度上の扱いを考えるときにも、このような作用の考え方は重要です。なぜなら、どのようなメカニズムで効果が期待されるのかが、保険上の分類や価格評価の前提にも関わるためです。
スライド5:投与方法と医療提供体制
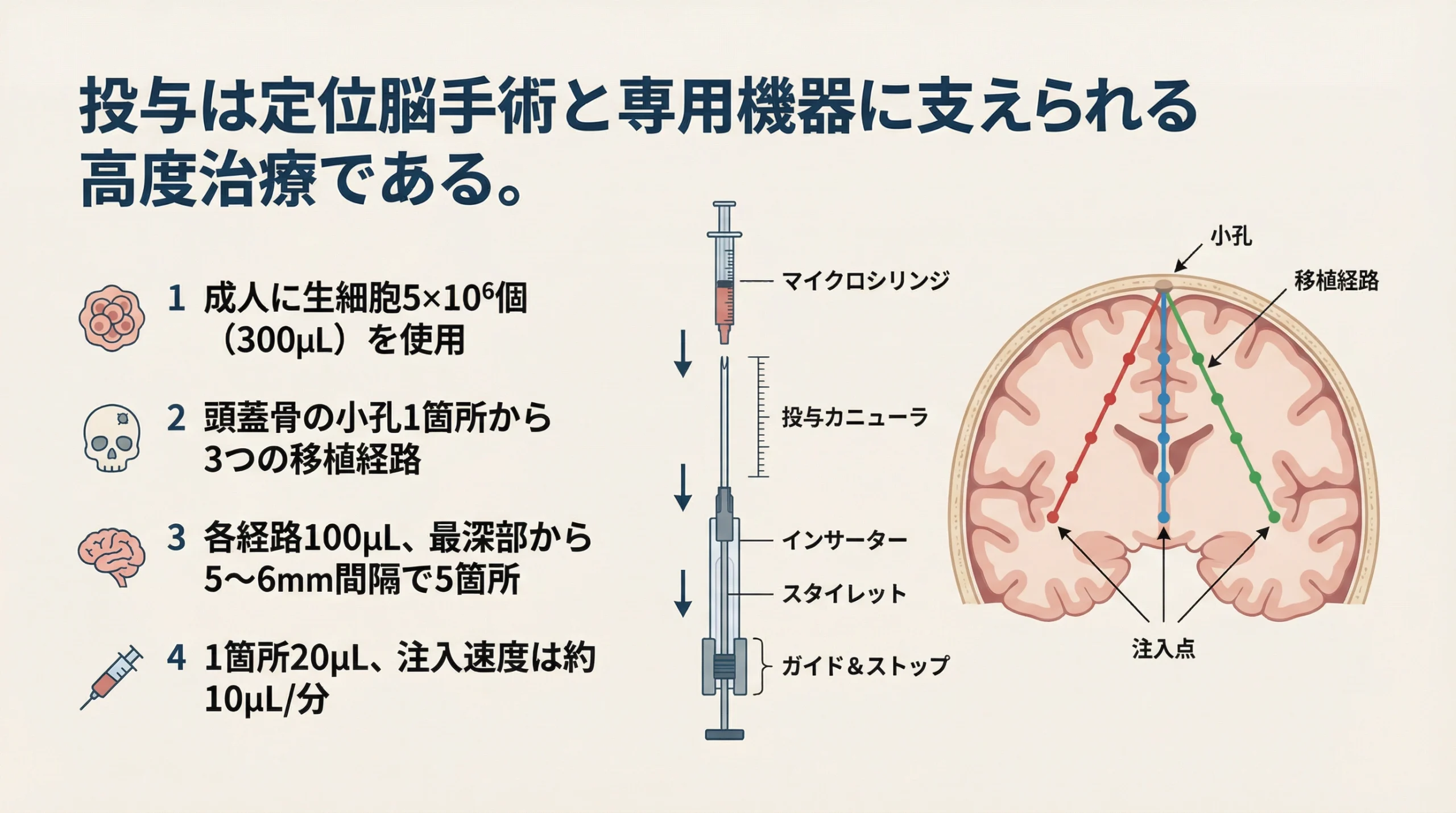
アクーゴの使用方法は、一般的な注射薬とは大きく異なります。資料では、成人に対し生細胞5×10^6個(300µL)の細胞調製液を用い、専用投与機器セットを用いた定位脳手術により、損傷組織周辺部へ移植するとされています 1。さらに、頭蓋骨の小孔1箇所を通し、3つの移植経路から投与し、1経路あたり100µLを、最深部から5〜6mm間隔で5箇所に、1箇所20µLずつ注入する方法が示されています 1。注入速度は約10µL/分です 1。
| 投与関連項目 | 内容 |
|---|---|
| 使用細胞数 | 生細胞 5×10^6個 |
| 使用量 | 300µL |
| 手技 | 専用機器セットを用いた定位脳手術 |
| 移植経路 | 3経路 |
| 1経路あたり | 100µL |
| 分割投与 | 5箇所に20µLずつ |
| 注入速度 | 約10µL/分 |
このスライドから分かるのは、アクーゴが製品の性能だけでなく、手技の精度と実施体制にも強く依存する治療だということです。言い換えれば、薬を処方するだけで完結する治療ではなく、脳外科的な対応力、施設体制、術者の経験が治療成立の前提になります。そのため、承認条件や保険上の議論でも、単純な薬剤費だけではなく、どのような医療資源を必要とする治療なのかを踏まえた理解が必要になります 1。
スライド6:有効性データの見方

中医協資料で最も注目されるのが、有効性データです。主要評価項目は、本品移植後又は偽手術実施後24週目におけるFMMSスコアのベースラインからの変化量でした 1。主たる比較は、各用量群を併合したSB623群と偽手術群との比較です 1。
| 指標 | SB623群 | 偽手術群 | 群間差 | 95%信頼区間 | p値 |
|---|---|---|---|---|---|
| 24週時点FMMS変化量 | 8.3±10.6 | 2.3±4.7 | 6.0 | 0.3–11.8 | 0.0401 |
資料では、この主要評価項目について統計学的に有意差が認められたとされています 1。慢性期の運動麻痺という改善が難しい領域で差が示された点は、制度上の評価に進むうえで非常に重要です。ただし、データの読み方としては慎重さも必要です。数値にはばらつきがあり、また「統計学的に有意であること」と「臨床現場でどの程度の意味を持つか」は、必ずしも同じではありません。それでも、中医協資料の整理においては、このデータが保険収載を議論する基礎資料になっていると理解できます 1。
スライド7:条件及び期限付承認とは何か
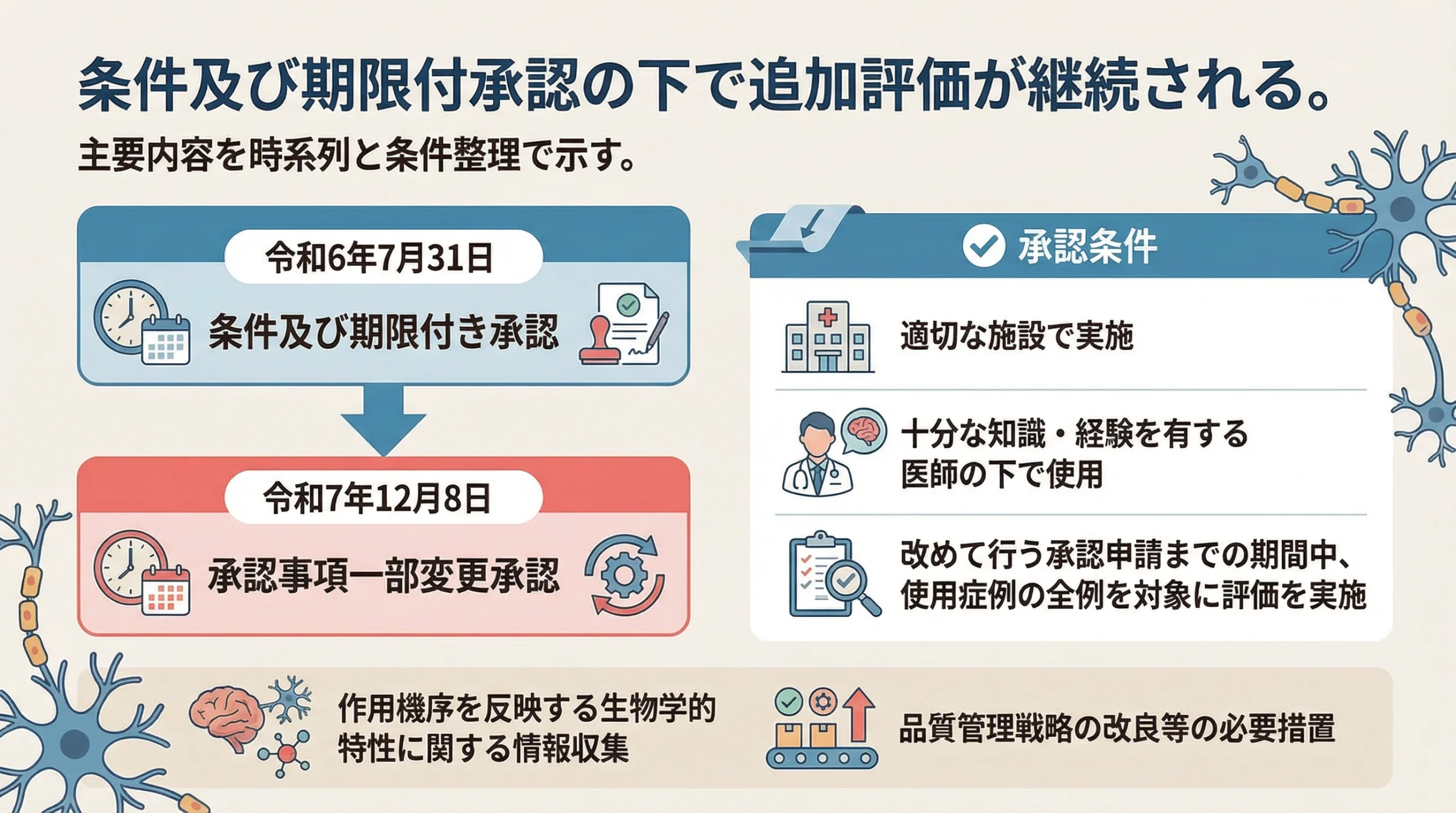
アクーゴは、令和6年7月31日に条件及び期限付承認を受け、その後令和7年12月8日に承認事項一部変更承認を受けています 1。ここで重要なのは、「承認された」という事実だけでなく、追加的な評価や情報収集を前提とした承認である点です。
資料に記載された承認条件は、大きく三つに整理できます。第一に、緊急時に十分対応できる医療施設で、外傷性脳損傷の診断・治療および定位脳手術に十分な知識・経験を持つ医師が、臨床試験成績や有害事象等の知識を習得したうえで使用することです。第二に、条件及び期限付承認後から改めて行う製造販売承認申請までの期間中、本品使用症例の全例を対象に評価を行うことです。第三に、作用機序を反映する生物学的特性に関する情報を収集し、品質管理戦略改良等の必要措置を講じることです 1。
この仕組みは、再生医療等製品の特徴をよく表しています。革新的な治療である一方、承認時点で不確実性が完全になくなるわけではありません。そこで、患者アクセスを確保しつつ、市販後にも知見を積み上げる枠組みが取られています。アクーゴは、早期アクセスと継続評価の両立を象徴する案件だといえます。
スライド8:保険上はどう扱われるのか
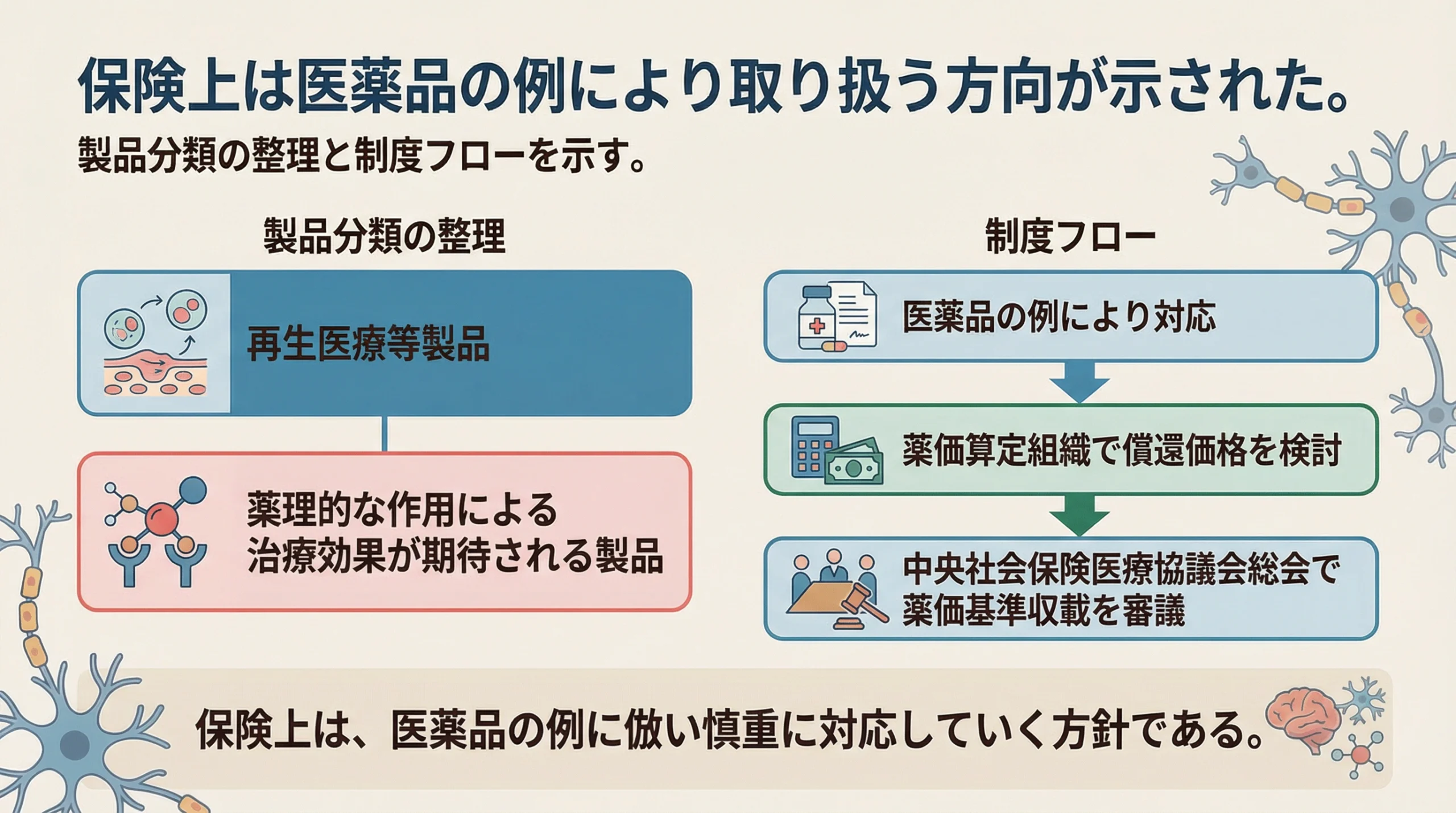
中医協資料では、アクーゴについて、医薬品と同様に薬理的作用による治療効果が期待される製品と整理し、医薬品の例により対応することが示されています 1。そのうえで、薬価算定組織で償還価格を検討し、中医協総会で薬価基準への収載を審議する流れが示されました 1。
この点は制度上とても重要です。再生医療等製品は、従来型の医薬品とも医療機器とも完全には一致しない側面を持ちます。しかし、保険実務では、個々の製品の作用や治療効果の考え方に応じて、既存の制度枠組みに位置づける必要があります。アクーゴについては、医薬品の例によって取り扱うという方向性が明示されたことで、薬価収載に向けた具体的なプロセスへ進むことになりました 1。
スライド9:この案件が示す政策的な含意
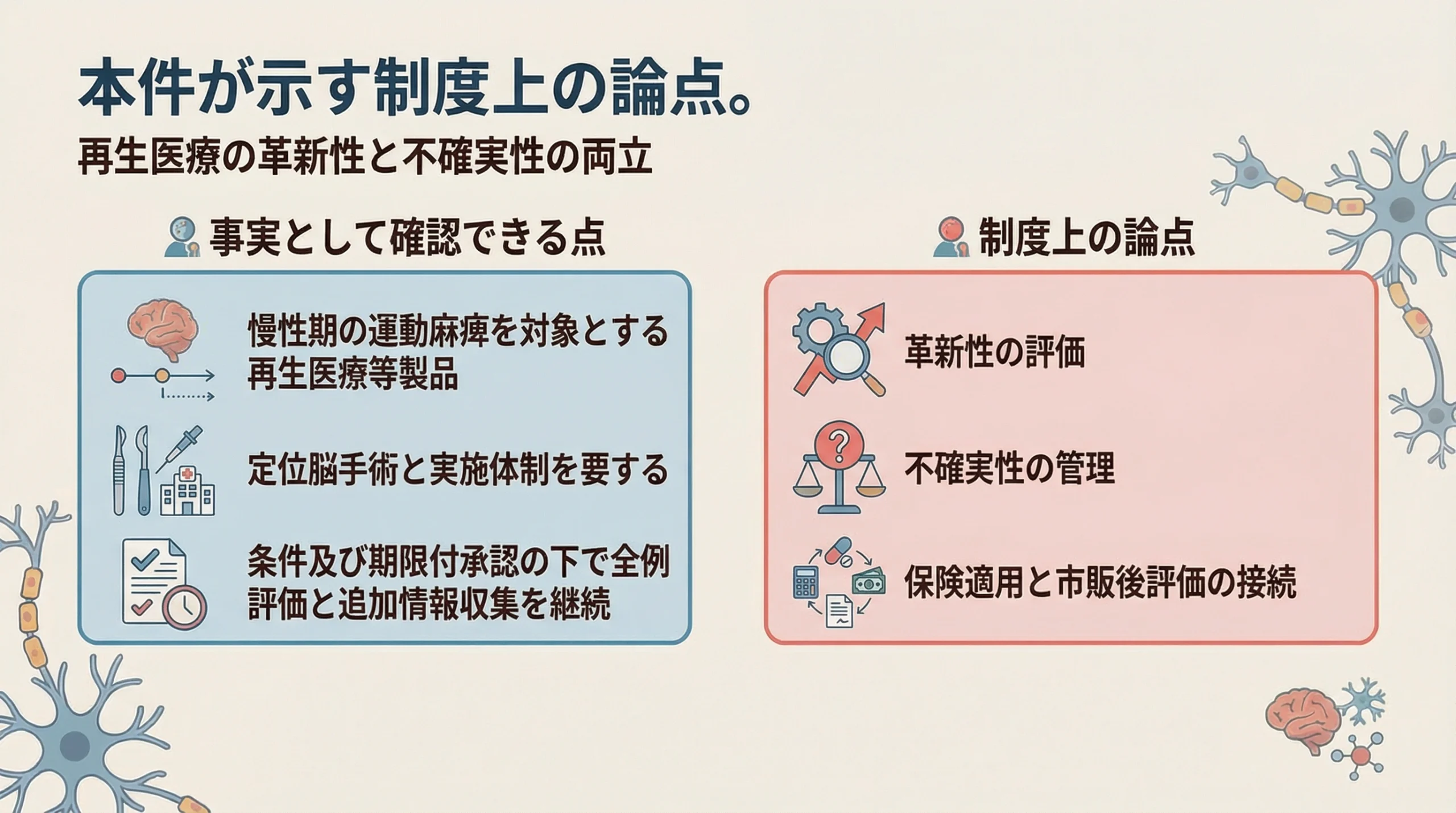
ここからは、資料の事実を踏まえた整理として、アクーゴが示す政策的な意味を考えます。アクーゴは、未充足ニーズの高い領域に対する新しい再生医療等製品であると同時に、高度な手術体制を要し、承認後にも継続評価を必要とする製品です 1。この二面性があるため、評価においては「期待が大きいから早く使えるようにすべき」という視点だけでも、「不確実性があるから慎重であるべき」という視点だけでも不十分です。
公的医療保険制度は、患者アクセス、医療の妥当性、財源の持続可能性という複数の要請を同時に満たさなければなりません。その意味で、アクーゴの案件は、再生医療のような新しい技術をどの段階で、どの条件で、どのように社会実装していくのかという問いを具体的に示しています。今後、類似の再生医療等製品が登場した際にも、アクーゴの取扱いは一つの参照点になる可能性があります。
スライド10:全体のまとめ
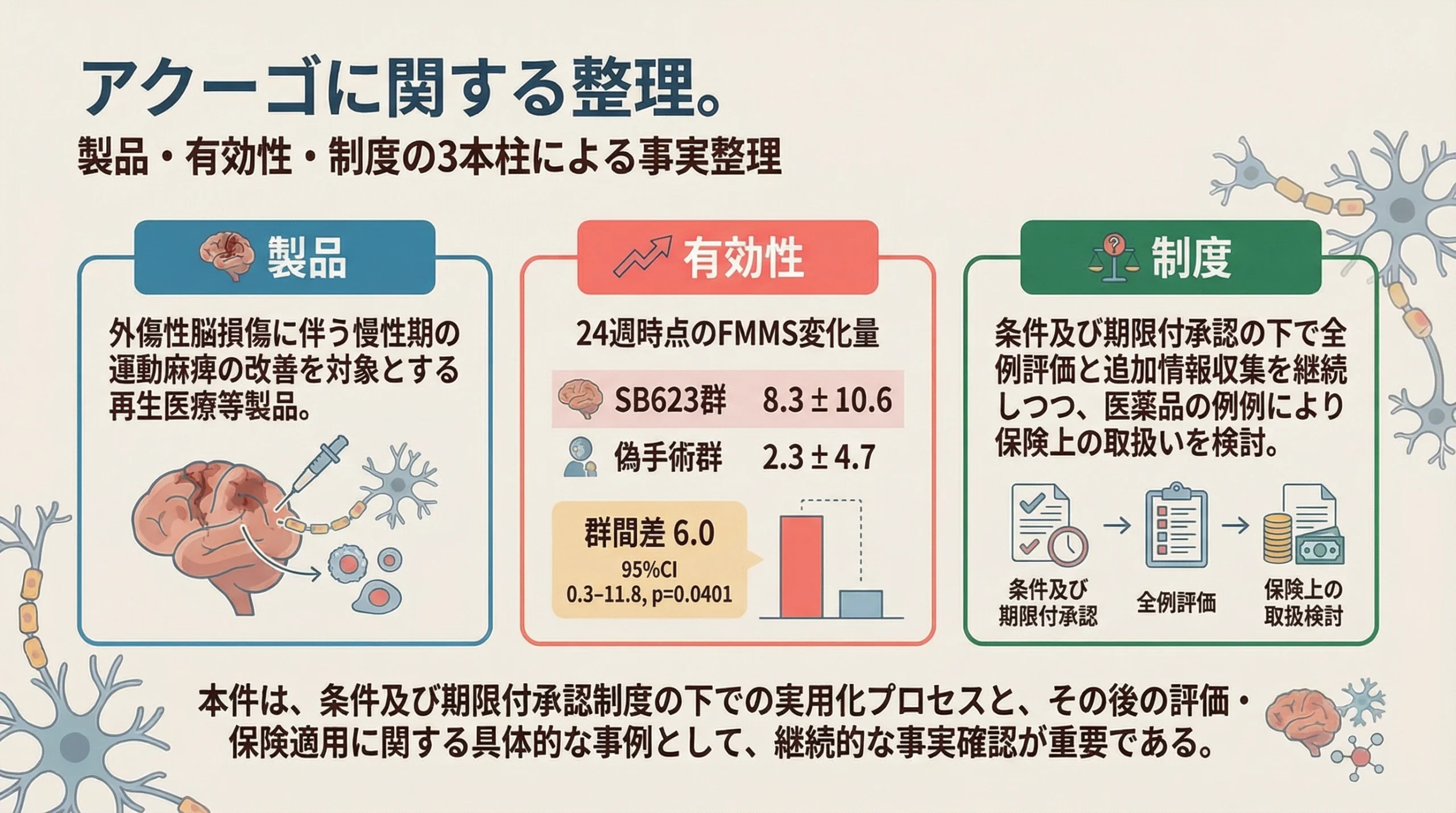
最後に全体を整理すると、アクーゴは、外傷性脳損傷に伴う慢性期の運動麻痺の改善を対象とする新再生医療等製品であり、遺伝子導入した間葉系幹細胞を脳内へ移植するという高い専門性を持つ治療です 1。作用としては、サイトカインを介した神経修復促進が期待され、24週時点のFMMS変化量では統計学的有意差が示されました 1。
一方で、この製品は条件及び期限付承認の下にあり、全例評価や作用機序に関する情報収集、品質管理戦略の改良といった追加的対応が求められています 1。そのような状況を踏まえて、中医協では、アクーゴを医薬品の例により対応する再生医療等製品として整理し、薬価基準収載の審議に進める方向が示されました 1。この案件は、製品評価、臨床的意義、制度設計が交差する好例であり、今後の再生医療政策を考えるうえでも注目に値します。
参考資料
本記事は、厚生労働省公開の中医協資料を主たる出典として作成しました。詳細確認の際は原資料をご参照ください。


コメント