本記事は、サンバイオが公表した2026年1月期決算説明会での質疑応答要約(2026年3月25日)をもとに、SB623(アクーゴ)の国内商業化と米国開発の現在地を、投資家向けに整理した解説記事です。出典はサンバイオIRの「よくあるご質問・お問い合わせ」です。[1]
結論:今回のQ&Aで見えた全体像
今回のQ&A全体を一言でまとめるなら、国内では商業化直前、米国では開発再加速直前という構図です。国内では、薬価収載の時期について会社側が2026年5月頃を想定していると説明し、当局との大きな認識齟齬もないと述べました。[1] 一方、米国ではFDAと試験デザインについて合意済みで、現在はプロトコル合意を目指しながら治験開始準備を進めている段階です。[1]
このため、SB623をめぐる投資判断では、国内は収載後の立ち上がり速度、米国は開始時期と費用増加のバランスが重要な評価軸になる局面に入ったと考えられます。
今回のQ&Aで押さえるべきポイント
| 論点 | 会社説明の要旨 | 投資家にとっての意味 |
|---|---|---|
| 国内薬価収載 | 2026年5月頃の収載を想定 | 制度面のハードルは終盤に近づいている |
| 当局との認識 | 大きな認識の齟齬はない | 価格交渉の対立懸念は一定程度後退 |
| 初年度の課題 | 供給より患者導線の見極めが重要 | 立ち上がり速度は医療現場での実装力次第 |
| 売上予想 | 薬価未収載のため売上は非開示 | 収益より先に販管費が立つ構造 |
| 米国Phase 3 | 試験デザインはFDAと合意済み | 開始前の具体準備フェーズに入っている |
| 米国費用 | 準備費用は一部織り込み済み | 前倒し開始なら研究開発費増加の可能性 |
サンバイオの2026年1月期決算説明会Q&Aとは何か
サンバイオはIRサイトの「よくあるご質問・お問い合わせ」の中で、2026年1月期決算説明会での質疑応答要約を公開しています。[1] 今回の開示は、決算資料そのものでは補足しきれない投資家の関心事項に対して、会社がどのような温度感で答えているかを知るうえで重要です。
とくにSB623(アクーゴ)は国内で慢性期外傷性脳損傷を対象とする製品として注目度が高く、質疑応答でも薬価収載の時期、上市初年度の立ち上がり、売上計上の考え方、米国Phase 3試験の開始準備が中心テーマになっていました。[1]
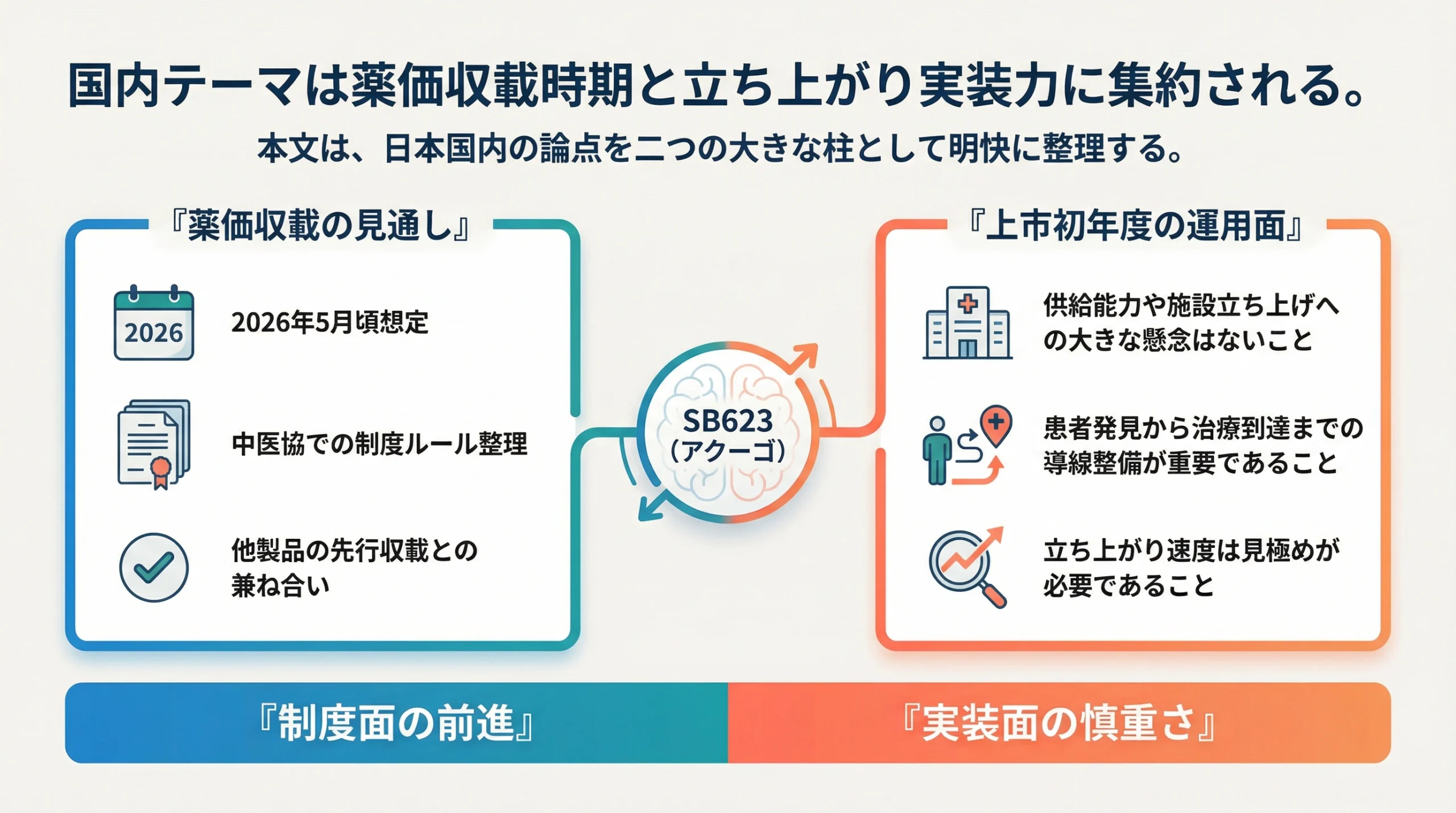
国内薬価収載はなぜ2026年5月頃と説明されたのか
中医協での制度整理が前提になっている
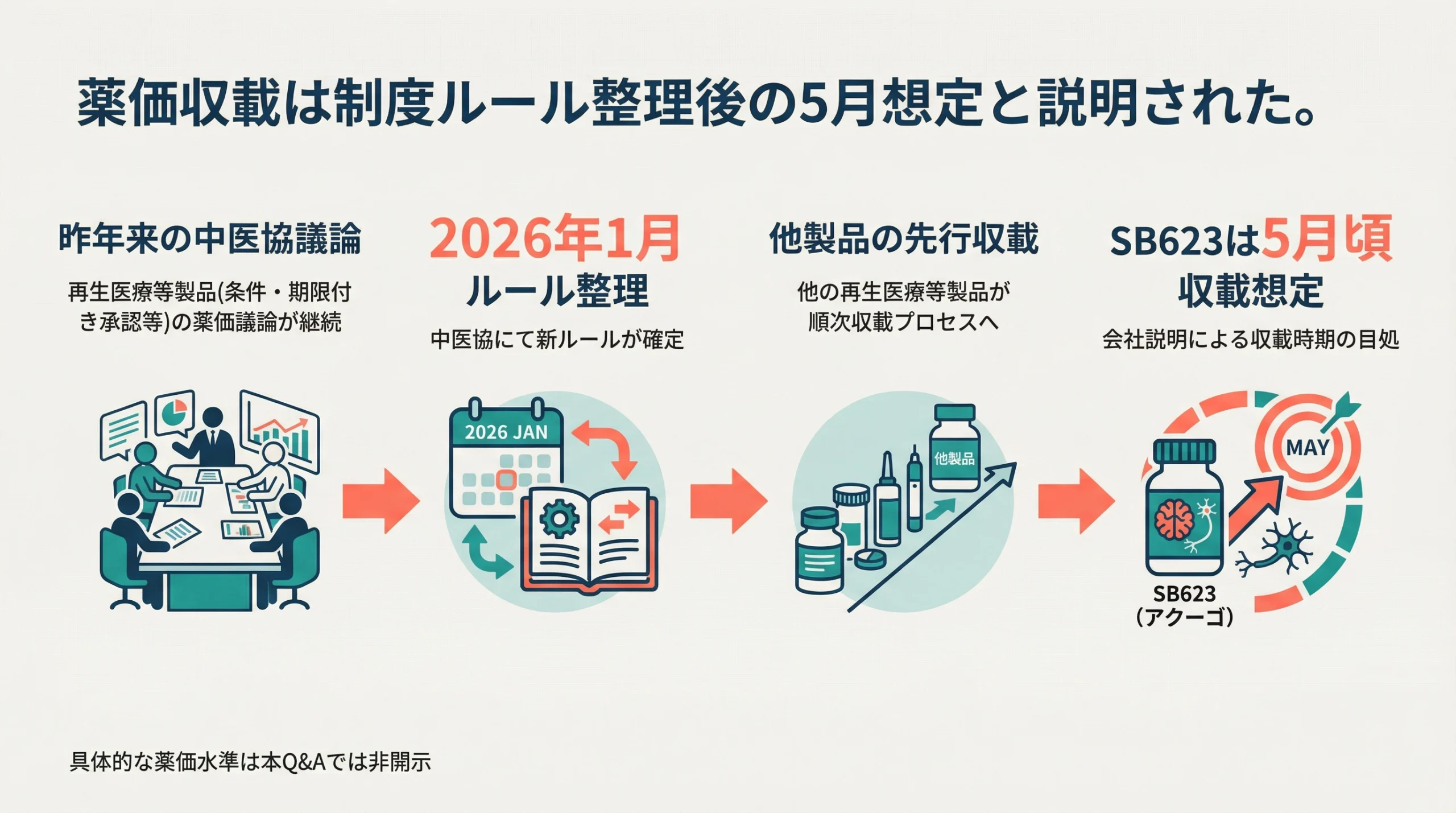
会社回答によれば、再生医療等製品、特に条件・期限付き承認製品の薬価については、昨年来、中医協で議論が続いており、2026年1月にルールが整理されたと説明されています。[1] 今回の5月見通しは、制度面の整理を前提に置いたタイミングといえます。
他製品の先行収載も時期見通しに影響
会社はあわせて、他の再生医療等製品の薬価収載が先行した兼ね合いもあり、同社製品の収載時期は5月頃になると想定していると述べています。[1] これは、制度整備が終わり、実際の収載待ちの段階に入ったと読むのが自然です。
「再生医療等製品、とりわけ条件・期限付き承認製品の薬価について、昨年来、中医協(中央社会保険医療協議会)で議論されてきましたが、今年1月にルールが整理されました。他の再生医療等製品の薬価収載が先行した兼ね合いもあり、当社製品の収載時期は5月頃になると想定しております。」— サンバイオ Q1回答 [1]
薬価について当局との認識のずれはあるのか
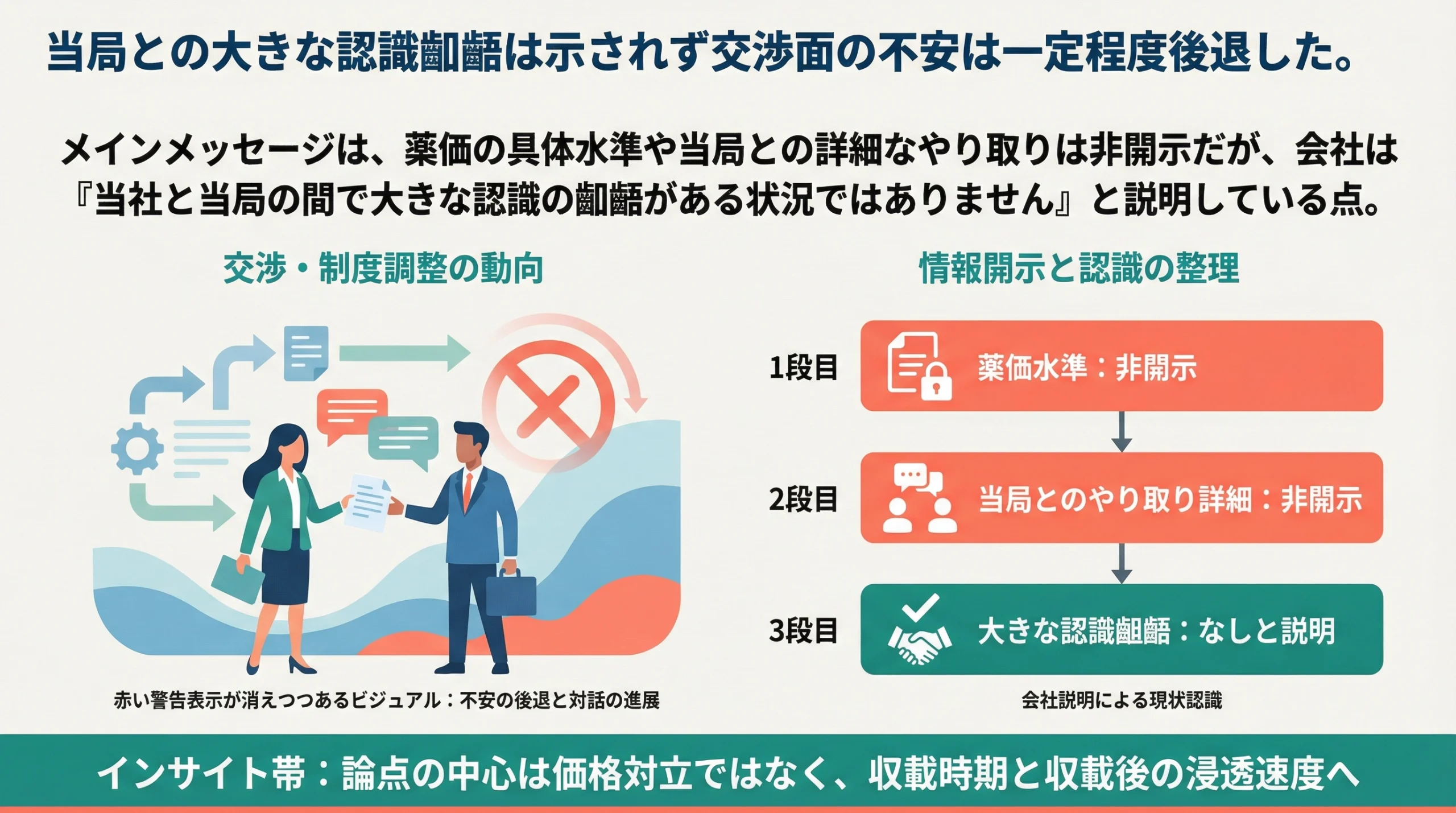
薬価の具体水準や当局とのやり取りの詳細は非開示とされましたが、会社は当社と当局の間で大きな認識の齟齬がある状況ではありませんと説明しました。[1] この表現は、価格面で大きな摩擦があるのではないかという市場の懸念を一定程度やわらげる内容です。
この回答を踏まえると、国内論点の重心は価格交渉そのものよりも、収載時期の確定と収載後の浸透速度へ移っていると考えられます。
「具体的な薬価や当局とのやり取りについては開示できませんが、当社と当局の間で大きな認識の齟齬がある状況ではありません。」— サンバイオ Q2回答 [1]
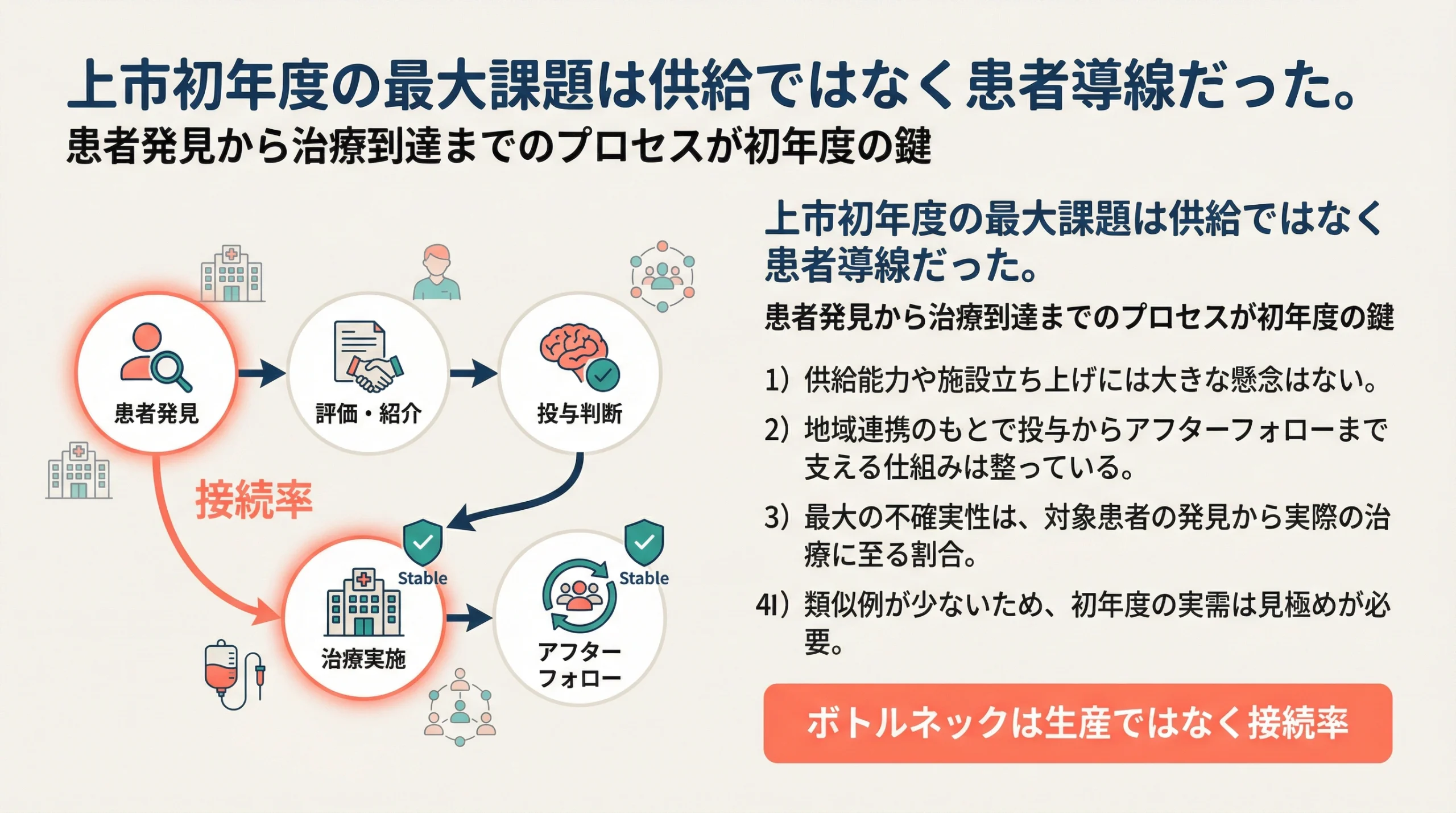
上市初年度の最大課題は何か
供給能力や施設立ち上げは大きな懸念ではない
会社は、上市初年度の立ち上がりにおける最大の課題について、供給能力や施設立ち上げについて大きな懸念はありませんと回答しています。さらに、地域と連携しながら対象患者の投与からアフターフォローまで支える仕組みは整っていると説明しました。[1]
本当の課題は患者発見から治療到達までの接続率
その一方で会社が不確実性として挙げたのは、患者さんの発見から実際に治療に至る割合です。類似する前例が少ないため、初年度の実需については現時点で見極めが必要としています。[1] つまり、SB623の初年度立ち上がりは、供給ではなく医療導線全体の実装力に大きく左右されるということです。
「供給能力や施設立ち上げについて大きな懸念はありません。地域と連携しながらアクーゴの対象となる患者さんを投与、アフターフォローまでサポートする仕組みは整っていますが、患者さんの発見から実際に治療に至る割合については類似する例が無いため現時点では見極めが必要な状況です。」— サンバイオ Q4回答 [1]

なぜ今期の業績予想では売上を計上していないのか
会社は、薬価が未収載であるため、現時点では売上高の開示を控えていると説明しています。[1] これは制度条件が確定する前に数値を出すことを避けていると理解するのが自然です。
一方で、販売体制構築や販促活動に必要な販管費については、既に予算に織り込んでいるとも回答しています。[1] このため、今期の損益構造は、収益より先にコストが立つ形になっています。
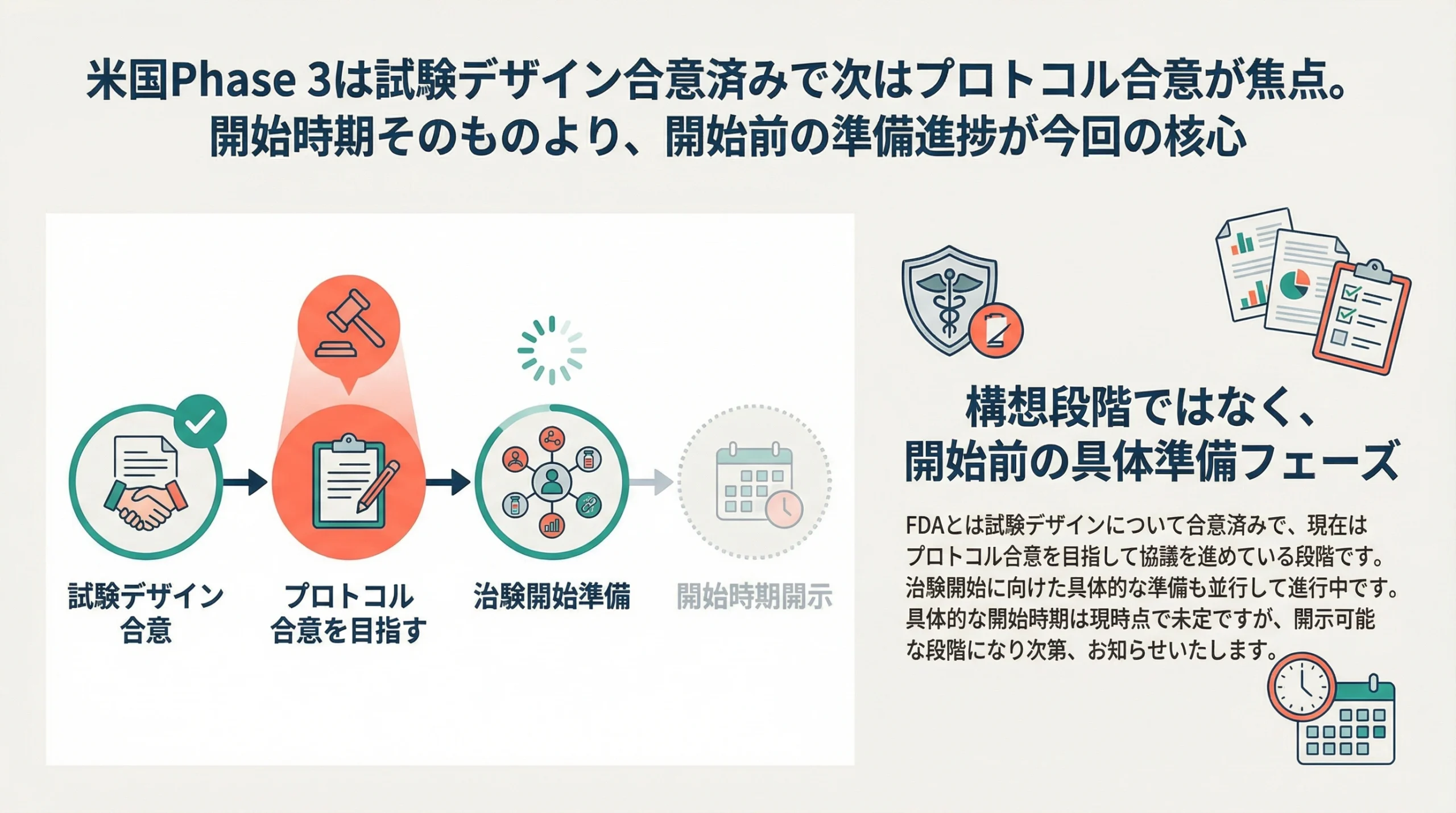
米国Phase 3試験はどこまで進んでいるのか
FDAとは試験デザインについて合意済み
会社は、FDAとは試験デザインについて合意していると回答しています。[1] これは米国開発が抽象的な構想段階ではなく、一定の設計レベルで前進していることを示す重要な情報です。
現在はプロトコル合意を目指して準備中
会社は続けて、現在はプロトコルの合意を目指し、治験開始に向けた準備を進めていると説明しました。開始時期については、開示可能な段階になり次第知らせるとしており、具体日程はまだ示されていません。[1]
「FDAとは試験デザインについて合意しており、現在はプロトコルの合意を目指し、治験開始に向けた準備を進めています。開始時期については、開示可能な段階になり次第、お知らせします。」— サンバイオ Q7回答 [1]
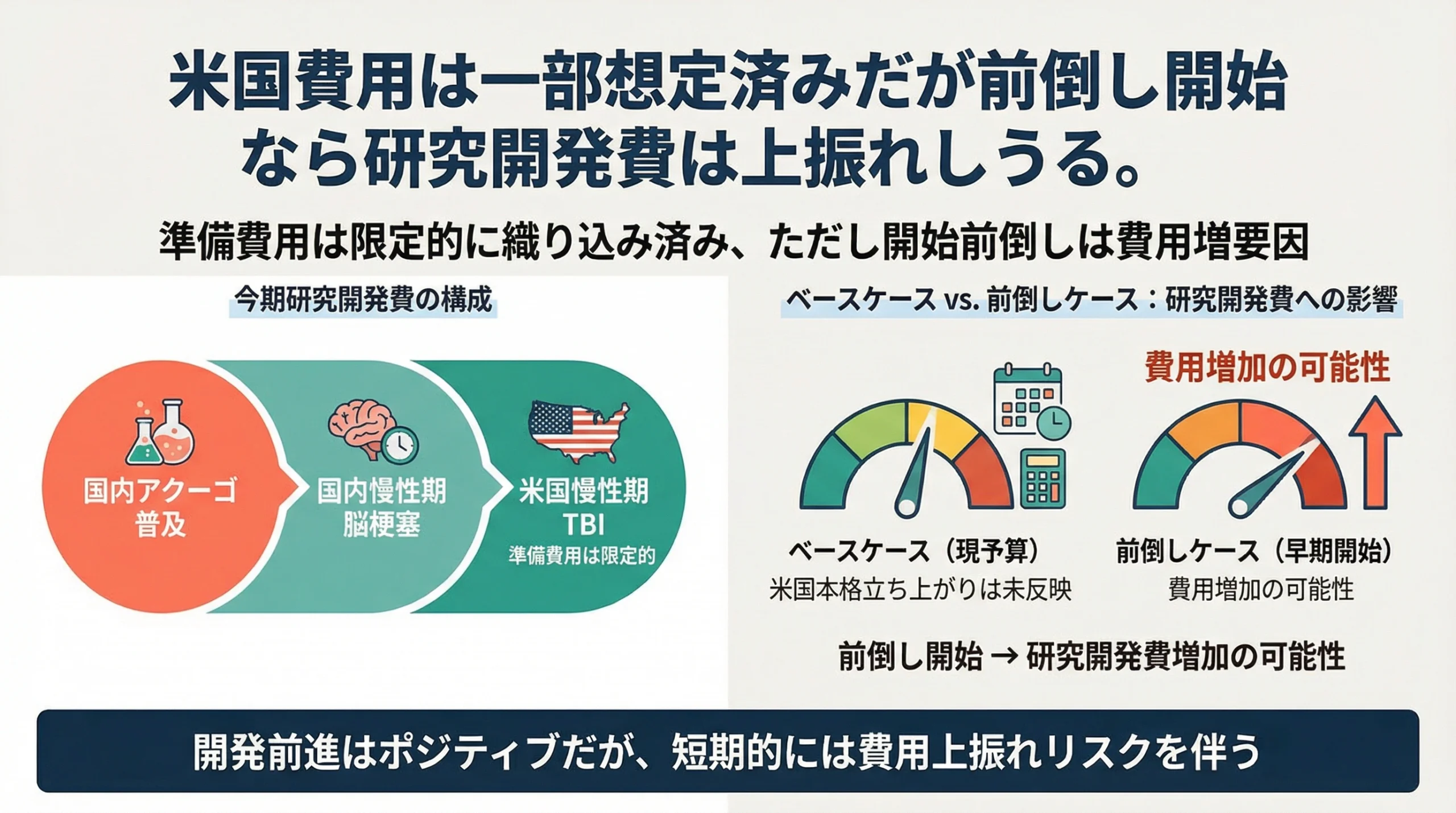
米国Phase 3費用は今期予算にどこまで織り込まれているのか
会社は、今期の研究開発費予算には、国内でのアクーゴの普及、国内慢性期脳梗塞プログラム、米国慢性期TBIプログラムの3つの要素が含まれていると説明しています。[1]
そのうえで、アメリカのPhase 3試験準備費用は現段階ではそれほど多く織り込んでいないとし、試験開始が前倒しとなった場合には研究開発費が増加する可能性があると述べました。[1] 今後は、開発前進のスピードと費用上振れのバランスが重要な観察ポイントになります。
「今期の研究開発費の予算には、国内でのアクーゴの普及、国内慢性期脳梗塞プログラム、米国慢性期TBIプログラムの3つの要素が含まれています。アメリカのPhase3試験準備費用は現段階ではそれほど多く織り込んでいませんが、試験開始が前倒しとなった場合には研究開発費が増加する可能性があります。」— サンバイオ Q8回答 [1]
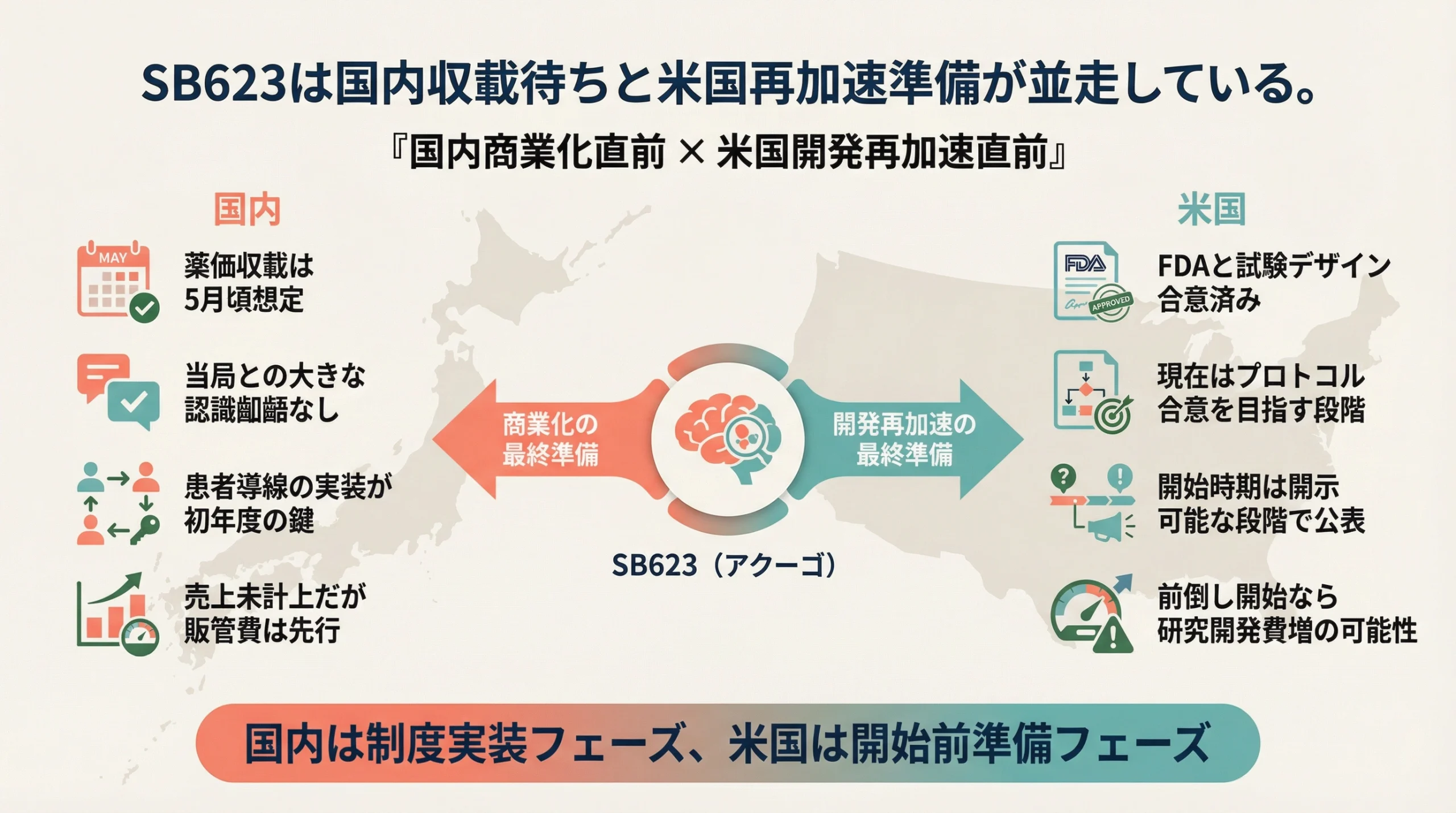
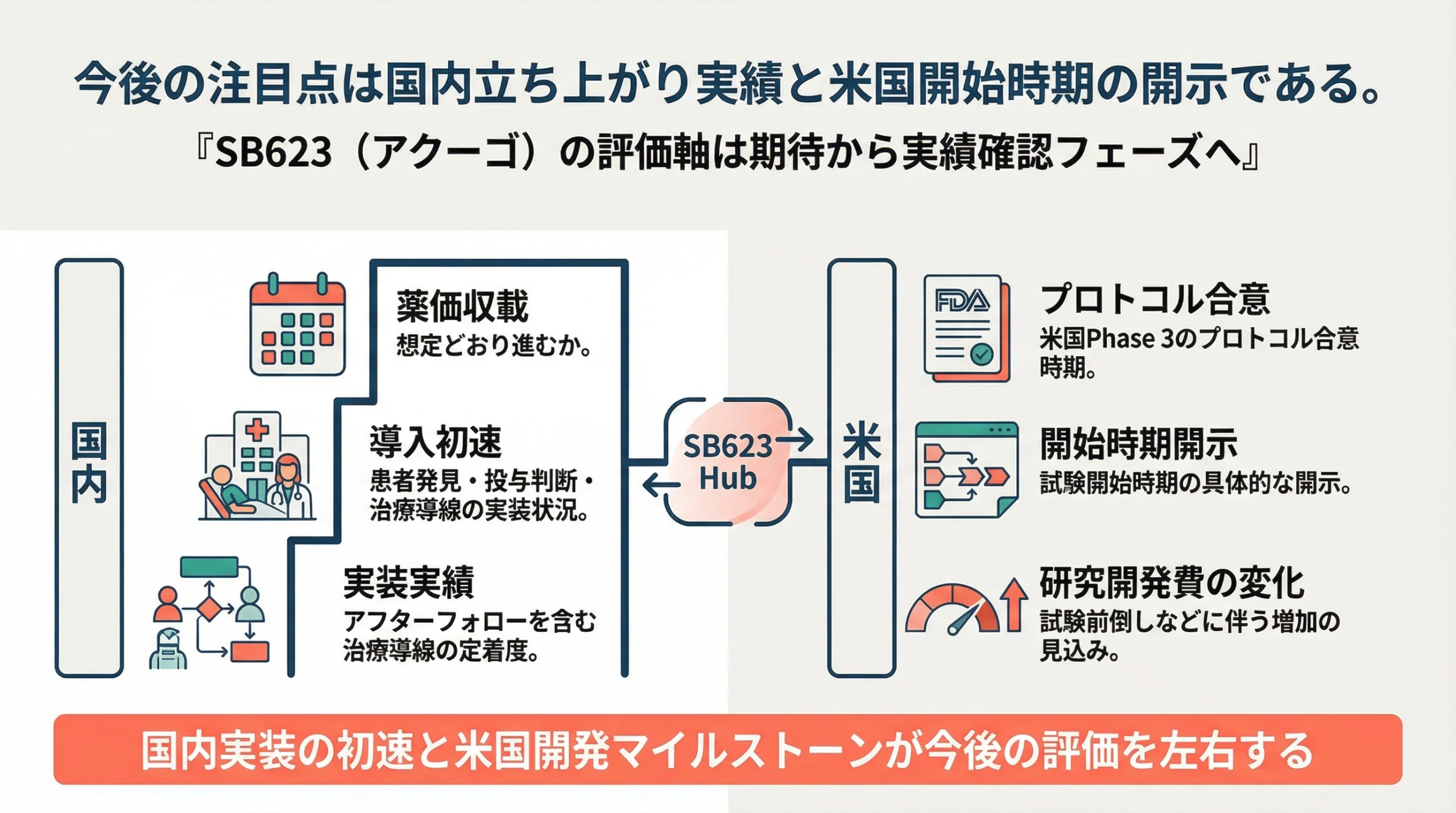
今後の注目点
今後、国内で最も重要になるのは、薬価収載が想定どおり進むか、そして収載後にどの程度のスピードで患者導入が進むかです。とくに患者発見、紹介、適応判断、治療実施、アフターフォローが現場でどれほど滑らかに回るかという、治療導線の運用実績が初年度評価の中核になります。
米国については、プロトコル合意がいつ見えてくるか、そしてPhase 3開始時期がいつ開示されるかが焦点です。開発が前進すれば期待は高まりやすい一方、短期的には研究開発費の増加も伴うため、どの条件で始まり、どの程度の費用インパクトを伴うのかまで含めて確認する視点が必要です。
まとめ
サンバイオの2026年1月期決算説明会Q&Aは、SB623(アクーゴ)について、国内と米国の二つの重要な進捗を示しました。国内では、薬価制度面の整理を経て、2026年5月頃の薬価収載を想定していることが示され、当局との大きな認識齟齬もないと説明されています。[1] 一方で、上市初年度の最大課題は供給ではなく、患者が実際に治療へ到達する導線の構築であることも明確になりました。[1]
また米国では、FDAと試験デザインについて合意済みであり、現在はプロトコル合意を目指しながら治験開始準備を進めている段階です。[1] ただし、開始時期はまだ未開示であり、前倒し開始となれば研究開発費が増加する可能性もあります。[1]
総じて言えば、今回のQ&Aは、SB623が単なる期待先行のテーマではなく、国内では商業化の現実フェーズ、米国では開発再加速の現実フェーズに入りつつあることを示した内容でした。



コメント